Физика | 10 - 11 классы
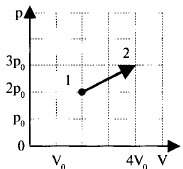
На pV — диаграмме изображен процесс перевода газа, совершенный с одним молем идеального одноатомного газа.
Чему равно количество теплоты, переданное газу при переходе из состояния 1 в состояние 2?
P0 = 0, 1 МПа, V0 = 2л.

Идеальный одноатомный газ совершает переход из состояния 1 в состояние2 изобарно?
Идеальный одноатомный газ совершает переход из состояния 1 в состояние
2 изобарно.
Количество теплоты, подведённое к системе в этом процессе, равно
225 кДж.
При этом внутренняя энергия газа?

Одноатомный идеальный газ в количестве 4 моль поглощает количество теплоты Q?
Одноатомный идеальный газ в количестве 4 моль поглощает количество теплоты Q.
При этом температура газа повышается на 20 К.
Работа, совершаемая газом в этом процессе, равна 1 кДж.
Чему равно поглощенное количество теплоты?

Даю 30 б?
Даю 30 б!
Идеальный одноатомный газ совершает переход из состояния 1 в состяние 2 изобарно.
Количество теплоты, подведенное к системе в этом процессе, равно 225 кДж.
При этом внутренняя энергия газа равна 135 кДж , но как получилось?

Одноатомный идеальный газ нагрели изобарно?
Одноатомный идеальный газ нагрели изобарно.
Переданное количество теплоты равно 50 Дж.
Найти изминение внуьренней энергии газа.

Идеальный одноатомный газ совершает переход из состояния 1 в состояние2 изобарно?
Идеальный одноатомный газ совершает переход из состояния 1 в состояние
2 изобарно.
Количество теплоты, подведённое к системе в этом процессе, равно
225 кДж.
При этом внутренняя энергия газа?

На рисунке изображён график изменения состояния одноатомного идеального газа в количестве 20 моль?
На рисунке изображён график изменения состояния одноатомного идеального газа в количестве 20 моль.
Какая температура соответствует состоянию 2, если в состоянии 1 она равна 300 К?

Внутренняя энергия одноатомного идеального газа в ходе изобарного процесса изменилась на 750дж?
Внутренняя энергия одноатомного идеального газа в ходе изобарного процесса изменилась на 750дж.
Найдите : а) работу, совершенную газом.
Б) количество теплоты полученное газом.

Два моля идеального одноатомного газа сначала изобарно нагрели, а затем, изохорно охладили до первоначальной температуры при этом давление газа уменьшилось в три раза (см?
Два моля идеального одноатомного газа сначала изобарно нагрели, а затем, изохорно охладили до первоначальной температуры при этом давление газа уменьшилось в три раза (см.
Рис. ).
После этого система изотермически вернулась в начальное состояние.
Начальная температура газа равна Т1 = 400 К.
Какое количество теплоты получил газ за весь процесс?

В процессе изохора одноатомному идеальному газу дали 600 Дж тепла?
В процессе изохора одноатомному идеальному газу дали 600 Дж тепла.
Газ остудился (в процессе изобара ).
Количество тепла выделенная в окружающую среду когда газ дошел до начального состояние ?
1000Дж.

Газ переводят из состояния 1 в состояние 3 так, как показано на p - V - диаграмме?
Газ переводят из состояния 1 в состояние 3 так, как показано на p - V - диаграмме.
Чему равна работа, совершенная газом в процессе 1 - 2 - 3, если р0 = 50 кПа, V0 = 2 л?
На этой странице находится вопрос На pV — диаграмме изображен процесс перевода газа, совершенный с одним молем идеального одноатомного газа?, относящийся к категории Физика. По уровню сложности данный вопрос соответствует знаниям учащихся 10 - 11 классов. Здесь вы найдете правильный ответ, сможете обсудить и сверить свой вариант ответа с мнениями пользователями сайта. С помощью автоматического поиска на этой же странице можно найти похожие вопросы и ответы на них в категории Физика. Если ответы вызывают сомнение, сформулируйте вопрос иначе. Для этого нажмите кнопку вверху.





Po = 0.
1 * 10 ^ 6 Па Vo = 2 * 10 ^ - 3 м3 Q = ?
= = =
p1 = 2 * po V1 = 2 * Vo
p2 = 3 * po V2 = 4 * Vo (из графика)
Q = ΔU + A
ΔU = U2 - U1 = (3 / 2) * (p2 * V2 - p1 * V1) = (3 / 2) * (3po * 4Vo - 2po * 2Vo) = 12 * po * Vo
A = (p1 + p2) * (V2 - V1) / 2 = 5 * po * Vo
Q = 12 * po * Vo + 5 * po * Vo = 17 * po * Vo = 17 * 0.
1 * 10 ^ 6 * 2 * 10 ^ - 3 = 3.
4 * 10 ^ 3 Дж (3, 4 кДж) = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =.